Průkopnická práce Nigra et al. z roku 1974 poprvé prokázala, že kompletní regrese nádorů anu lze dosáhnout radioterapií s konkomitantní chemoterapií mitomycinem nebo porfyromycinem. Samostatná chemoradioterapie, tzn. konzervativní léčba zachovávající svěrač, se stala standardní terapií u většiny stadií. Výsledky byly natolik přesvědčivé, že k zavedení tohoto standardu nebylo třeba srovnávacích studií.
Další výzkum se proto zaměřil na vývoj chemoradiačního schématu, určení dávky záření, frakcionace a rozsahu cílového objemu a dále na otázku adjuvantní terapie navazující na primární chemoradiaci.
Benefit nepřerušeného režimu ozařování
Současný léčebný standard se opírá o výsledky šesti velkých randomizovaných studií z přelomu milénia (EORTC 22861, RTOG 87-04, RTOG 98-11, ACCORD 03, UCCCR ACT I, CRUK ACT II). Primárním cílem všech bylo najít optimální protokol chemoradioterapie. V neobvykle rozsáhlé britské studii fáze III UK ACT II se potvrdil dříve uvedený závěr studie RTOG 98-11, že ve vlastní chemoradiaci není žádný významný rozdíl mezi režimem s cisplatinou a 5-fluorouracilem (CDDP + 5-FU) a s mitomycinem C a 5-fluorouracilem (MMC + 5-FU). Nepodařilo se také prokázat benefit adjuvantní terapie dvěma cykly režimu CDDP + 5-FU následujícího po chemoradioterapii.
Dávky záření byly předmětem více studií, převážně nerandomizovaných. Prokazují signifikantní snížení rizika lokálního relapsu při zvýšení dávky nad 50 Gy, při postižení regionálních uzlin při dávkách nad 54 Gy. Více studií (RTOG 98-11, ACT II aj.) prokazuje benefit nepřerušovaného režimu ozařování, přestože přerušované („split“) režimy chemoradioterapie vycházely z předpokladu snížení extenzivní toxicity, jež se vyskytovala při dávkách nad 50 Gy. Více studií také prokazuje přirozeně očekávaný efekt – snížení rizika relapsu při dodržení kontinuálního režimu frakcionovaného ozařování a absenci jakýchkoliv přerušení.
Z uvedené řady studií vychází současný standard terapie – ozáření primárního nádoru anu a spádových lymfatik do celkové dávky 54–60 Gy (1,8–2 Gy/frakce, 5 frakcí/týden) s konkomitantní chemoterapií režimem MMC + 5-FU nebo CDDP + 5-FU. Touto terapií bylo v rámci studií dosaženo kompletní regrese do 90 %, pětiletého přežívání do 70 % a pětiletého přežívání bez relapsu do 70 %.
Infuzní 5-FU lze nahradit kapecitabinem. Ve dvou publikovaných retrospektivních studiích byla prokázána stejná účinnost režimů MMC + 5-FU a MMC + kapecitabin. Ten se podává ve stejném režimu, jaký byl ověřen v předoperační chemoradiaci Ca rekta – 825 mg/m2 2× denně po celou dobu ozařování. Přestože nejsou studie randomizované, lze je považovat za dostatečné při průkazu non-inferiority.
Nalezení bezpečnější techniky záření...
Zásadním problémem chemoradioterapie nádorů anu byla a je akutní i chronická toxicita. Frekvence akutních nežádoucích účinků (stupně 3 a 4) přesahuje v některých souborech 80 %. Inguinální a perianální dermatitidy a proktitidy stupně 3 a 4 jsou uváděny s frekvencí do 40 %. Leukopenie, resp. neutropenie stupně 4 je ojediněle uvedena s frekvencí až 34 %, akutní gastrointestinální toxicita stupně 3 a 4 s frekvencí do 15 %. Mortalita v přímé souvislosti s terapií dosahuje 2 %. Akutní toxicita přináší vysoké riziko přerušení režimu chemoradioterapie.
Frekvence pozdních nežádoucích účinků dosahuje až 20 %. Zahrnují anální ulcerace, fistulace (např. rektovaginální), vaginální stenózy, anorektální stenózy, dysfunkce svěrače a poruchy kontinence. Pozdní efekty někdy vyžadují zavedení stomatu.
Cestou k redukci závažné a časté toxicity je zavedení dokonalejší techniky aplikace záření, resp. radioterapie s modulovanou intenzitou (intensity modulated radiation therapy, IMRT). Několik studií prokazuje signifikantní redukci rizika akutních nežádoucích účinků a zároveň signifikantní redukci počtu nutných přerušení režimu při zachování dávek v cílovém objemu.
Přímé srovnání technik trojrozměrné konformní radioterapie (3-dimensional conformal radiation therapy, 3D-CRT) a IMRT nabízí studie RTOG 0529, možná s kontroverzními výsledky. Nezdařilo se sice prokázat původní hypotézu (redukce toxicity stupně 2 o 15 % a více), přesto jsou ale výsledky studie přesvědčivé. Je totiž patrná významná redukce toxicity stupně 3.
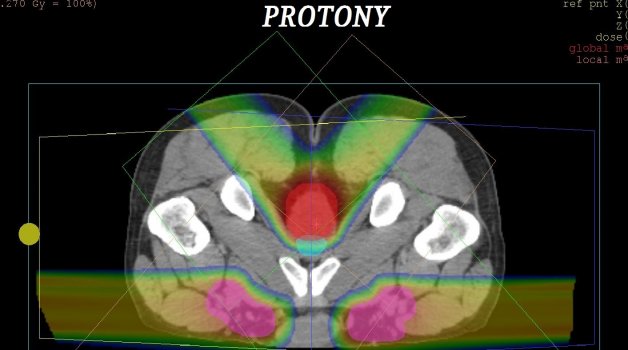
Další redukce toxicity lze dosáhnout i protonovou radioterapií, která je od konce roku 2012 dostupná v ČR. V roce 2015 byly publikovány dvě významné práce, které prokazují další dávkovou redukci při radioterapii standardního objemu u Ca anu, opět významnou. To je výsledek do jisté míry očekávaný.
... a redukce dřeňové toxicity
Přínos prací spočívá i v hodnocení radiační zátěže dalšího rizikového orgánu, a to kostní dřeně pánve. Dávky v kostní dřeni nebyly v předchozích srovnáních IMRT vs. 3D-CRT hodnoceny ani nebyl zkoumán vztah dřeňové dávky k hematotoxicitě. Ta je přitom významná, ve 3.–4. stupni je referována u více než 50 % nemocných ve standardním režimu (viz výše). Určitou výjimkou je práce Lina et al., která prokazuje, že u techniky IMRT je dávka ve dřeni dokonce mírně vyšší než u techniky 3D-CRT. Zásadní problém techniky IMRT spočívá pak v tom, že má potenciál redukovat toxicitu gastrointestinální, genitourinární a kožní, nicméně ne dřeňovou (tu nejvýznamnější z hlediska dodržení léčebného režimu). Dozimetrické práce z roku 2015 prokazují statisticky významnou redukci dávek v kostní dřeni pánve, která dává podklad pro dobrou toleranci obligátní konkomitantní chemoterapie. Translace dozimetrických dat kostní dřeně do klinické výhody je patrná a klinická data očekávají další zpracování. Kvantifikace rizik myelotoxicity a dávek v kostní dřeni pánve není zatím součástí dostupných databází (např. QUANTEC), protože v běžném procesu plánování se dávky v kostní dřeni nekalkulují.
Summa summarum: U nádorů anu spočívá zásadní problém v toleranci léčby, adherenci k léčebnému režimu, resp. přerušování režimu. Protonová radioterapie metodou tužkového skenování (proton beam scanning, PBS) přináší dozimetrickou výhodu, která tyto otázky řeší. S lepší tolerancí i adherencí lze očekávat i vyšší účinnost chemoradioterapie.
Přirozeně nelze nijak rozporovat fakt, že účinnost chemoradioterapie IMRT je výborná, kompletní regrese se dosahuje v rozsahu 90 % i více. Naproti tomu je ale nutné připustit otázku, zda nemůže být ještě lepší při vyšší toleranci – tedy zda nezavést protonovou radioterapii metodou PBS jako standard.
Literatura u autora
MUDr. Pavel Vítek, Ph.D., MBA,